2000-10-18
Leif Andersson
Henriksbergsvägen 104
136 67 HANINGE
Tel 08/777 45 33
e-post leif.andersson@haninge.mail.telia.com
Hemsidor http://go.to/lean1
http://come.to/lean
Om vatten och ĺnga
Vi tänker oss en injektionsspruta med perfekt tätning mellan
kolv och sprutcylinder.
Doppa ner nĺlen i en skĺl med vatten.
Skjut in kolven sĺ att den inneslutna volymen blir noll.
Dra ut kolven sĺ att lite vatten sugs in i sprutan.Täta igen
nĺlen.
Om du nu snabbt drar ut kolven fĺr du vakum ovanför vattnet.
Men vattnet börjar nu övergĺ till ĺnga.Ĺngbildningen blir häftig.
Sĺ häftig att den inte bara sker vid vattenytan.Ĺngblĺsor bildas
även inne i vattnet,vattnet kokar.Ĺngtrycket ovanför vattnet
stiger tills vi fĺr ett jämviktsläge.
Om du nu sakta trycker in kolven och hĺller temperaturen konstant
förblir ĺngtrycket konstant.I stället för att trycket stiger när
du minskar volymen minskar ĺngvolymen genom att ĺnga kondenserar
sĺ att vattenmängden i sprutan ökar.
Vattenytan kan inte veta hur stor ĺngvolym som finns ovanför den.
Där frisätts och infĺngas vattenmolekyler.Ju högre temperaturen
är ju fler vattenmolekyler har sĺ stor rörelseenergi att de
förmĺr lämna vattenytan och ju högre trycket är ju fler vatten-
molekyler slĺr emot vattenytan sĺ häftigt att de infĺngas och
binds i vattnet.
Hĺller vi konstant temperatur blir alltsĺ frisättningen av vatten-
molekyler konstant.Ökar vi dĺ ĺngtrycket rubbar vi balansen
mellan frisättning och infĺngning.Fler vattenmolekyler infĺngas
än de som frisätts.Ĺnga kondenserar till vatten.Ĺngtrycket sjunker
tills vi pĺ nytt fĺr balans vid samma ĺngtryck som förut.
För varje temperatur finns alltsĺ ett ĺngtryck som ger balans
mellan ĺnga och vatten.Detta ĺngtryck kallas för mättnadstryck.
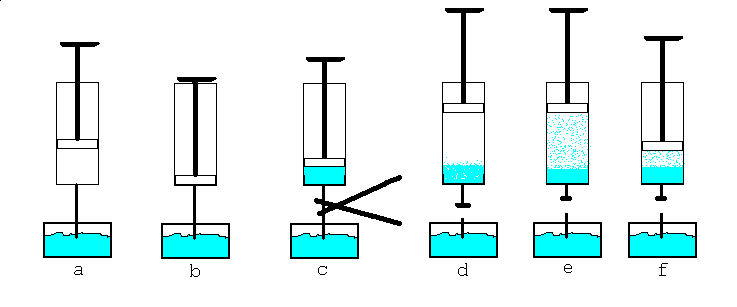 Fig 1
Fig 1
 Fig 2
Om du,när du drar ut kolven till läge d öppnar ett hĺl i kolven
sĺ att luft kan komma in kommer du att fĺ atmosfärstryck inne
i sprutan.Det medför att ĺngbildningen inte blir lika häftig.Om
temperaturen är under 373 K kommer vattenet inte att koka.Men
att vattenytan bombarderas med luftmolekyler pĺverkar inte
balansen mellan frisättning och bindning av vattenmolekyler.
Sĺ smĺningom kommer vi till att ĺngtrycket blir mättnadstrycket,
totala trycket blir atmosfärstryck och den torra luftens tryck
blir atmosfärstryck minus mättnadstryck.
Om du stänger hĺlet i kolven och skjuter in den komprimeras
luften praktiskt taget enligt allmänna gaslagen och ĺngtrycket
blir mättnadstrycket.Totala trycket i sprutan blir det resulterande
lufttrycket plus ĺngtrycket.
Fig 2
Om du,när du drar ut kolven till läge d öppnar ett hĺl i kolven
sĺ att luft kan komma in kommer du att fĺ atmosfärstryck inne
i sprutan.Det medför att ĺngbildningen inte blir lika häftig.Om
temperaturen är under 373 K kommer vattenet inte att koka.Men
att vattenytan bombarderas med luftmolekyler pĺverkar inte
balansen mellan frisättning och bindning av vattenmolekyler.
Sĺ smĺningom kommer vi till att ĺngtrycket blir mättnadstrycket,
totala trycket blir atmosfärstryck och den torra luftens tryck
blir atmosfärstryck minus mättnadstryck.
Om du stänger hĺlet i kolven och skjuter in den komprimeras
luften praktiskt taget enligt allmänna gaslagen och ĺngtrycket
blir mättnadstrycket.Totala trycket i sprutan blir det resulterande
lufttrycket plus ĺngtrycket.
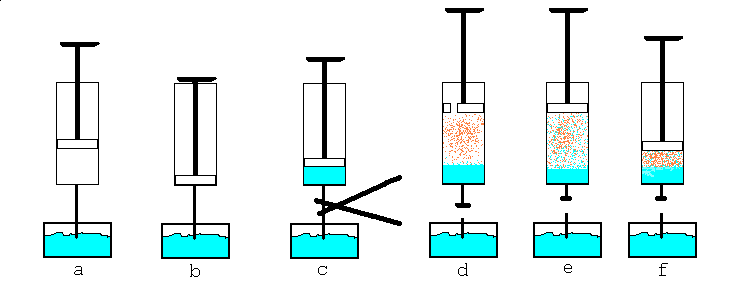 Fig 3
Den torra luften fyller ut den tillgängliga volymen.Vattenĺngan fyller
ut den tillgängliga volymen.Den torra luftens tryck och vattenĺngans
tryck adderas och summan blir den fuktiga luftens tryck.
Den torra luftens tryck kallas partialtrycket för den torra luften
och ĺngans tryck kallas ĺngans partialtryck.Det totala trycket är
summan av alla partialtryck.
Ĺngtrycket över en vattenyta är alltsĺ lika med mättnadstrycket,om
temperaturen har varit konstant sĺ länge att det rĺder balans mellan
förĺngning och kondensation vid vattenytan.Men för den luft som
omger oss avviker ĺngtrycket ofta frĺn mättnadstryck av tvĺ orsaker.
1 Det finns inget vatten i närheten som kan förĺngas
2 Temperaturen har nyligen ändrats
Om man sänker temperaturen hos luft sjunker mättnadstrycket för
vattenĺnga sĺ att det kan hamna under det ĺngtryck som finns i luften.
Vid 293 K är vattenĺngans mättnadstryck 2.4 kPa och tätheten för
mättad ĺnga är 17.5 g/m3.Men om luften bara innehĺller 40 % av den
vattenmängden d v s om ĺngans täthet bara är 0.4*17.5 = 7 g/m3 blir
även ĺngans tryck 40 % av mättnadstrycket d v s 1 kPa.Vi säger dĺ
att relativa fuktigheten är 40 %.Med realtiv fuktighet menas alltsĺ
vattenĺngans patialtryck i procent av vattenĺngans mättnadstryck.
Om vi har luft med 40 % relativ fuktighet vid temperaturen 293 K är
alltsĺ ĺngans tryck 1 kPa och varje m3 fuktig luft innehĺller 7 g
vatten.Sänker vi temperaturen sjunker mättnadstrycket vilket innebär
att den relativa fuktigheten stiger.Vid c:a 280 K blir mättnadstrycket
1 kPa vilket innebär att den relativa fuktigheten blir 100 %.
Detta sätt att räkna är inte helt korrekt eftersom tätheten för mättad
ĺnga inte är helt proportionell mot trycket.Ĺngtätheten vid 280 K är
7.8 och man kan faktiskt sänka temperaturen till 279 K innan man nĺr
100 % relativ fuktighet.Men för praktiska uppskattningar är metoden
oftast användbar.
Fortsätter vi att sänka temperaturen kommer vatten att kondensera.Det
kan ske vid en vattenyta men det är ocksĺ möjligt att vatten kondenserar
till smĺ droppar som svävar i luften.Luft med sĺdana smĺ droppar kallas
dimma eller moln.Den temperatur där vatten börjar falla ut i vätskeform
kallas för daggpunkten.
När vatten förĺngas (eller kondenserar) omsätts värme.Detta värme kallas
ĺngbildningsvärme och kan delas upp i tre delar:
1 När vatten övergĺr till ĺnga ökar volymen.Denna volymökning sker
vid mättnadstryck och innebär ett arbete PV där P=mättnadstryck
och V=volymökning.Detta arbete mĺste motsvaras av lika stor
energitillförsel i form av värme om temperaturen skall förbli
konstant.
2 När vattenmolekylerna lämnar vätskan kan de röra sig friare.Antalet
frihetsgrader d v s entropin ökar.För att hĺlla konstant temperatur
mĺste vi tillföra energi till dessa nya frihetsgrader.Vi mĺste
tillföra energin TS där T=temperaturen och S=entropiökningen.
3 Bindningarna mellan molekylerna i vätskan (eller isen) mĺste brytas
för att molekyler skall kunna lämna vätskan.Detta kräver värmetill-
försel.
1 kg vatten som förĺngas vid 293 K ger 58 m3 ĺnga vid 2.3 kPa (volymen
pĺ utgĺngsvätskan är försumbar).Volymökning pĺ 58 m3 vid 2.3 kPa ger ett
arbete pĺ 133 kJ.Men för att förĺnga detta vatten mĺste vi tillföra
ĺngbildningsvärmet d v s 2451 kJ.Det ĺtgĺr alltsĺ 2451 - 133 = 2318 kJ
för att öka antalet frihetsgrader och för att bryta molekylbindningar.
För att förĺnga 1 kg vatten vid 293 K mĺste man alltsĺ tillföra 2451 kJ värme
vid den konstanta temperaturen 293 K.Entropin hos detta tillförda värme blir
alltsĺ 2451/293 = 8.37 kJ/K.
Vatten är nödvändigt för allt liv och tillgĺng till vatten är alltsĺ en
förutsättning för att en plats skall vara beboelig.Och praktiskt taget
över allt pĺ jorden finns vatten tillgängligt i form av vattenĺnga i
luften.Även torr ökenluft innehĺller vatten.Med sĺ lĺg relativ fuktighet
som 10 % innehĺller het ökenluft vid 323 K (50 oC) 8 g vatten per m3.
En luftkonditioneringsanläggning för ett hus pĺ 200 m3 som ĺstadkommer
en halv luftomsättnig per timme hanterar 100 m3 per timme d v s
800 g vatten per timme.En sĺdan anläggning skulle alltsĺ kunna konden-
sera ut ett par hinkar vatten per dygn.Tillräckligt för ett hushĺlls behov
av dricksvatten.
För att underlätta uppskattningar av vattenupptag och vattenutfällning för
luft har jag kompletterat programmet för Allmänna gaslagen med uppskattningar
för fuktig luft (t v fungerar endast isokor och isoterm).
Fig 3
Den torra luften fyller ut den tillgängliga volymen.Vattenĺngan fyller
ut den tillgängliga volymen.Den torra luftens tryck och vattenĺngans
tryck adderas och summan blir den fuktiga luftens tryck.
Den torra luftens tryck kallas partialtrycket för den torra luften
och ĺngans tryck kallas ĺngans partialtryck.Det totala trycket är
summan av alla partialtryck.
Ĺngtrycket över en vattenyta är alltsĺ lika med mättnadstrycket,om
temperaturen har varit konstant sĺ länge att det rĺder balans mellan
förĺngning och kondensation vid vattenytan.Men för den luft som
omger oss avviker ĺngtrycket ofta frĺn mättnadstryck av tvĺ orsaker.
1 Det finns inget vatten i närheten som kan förĺngas
2 Temperaturen har nyligen ändrats
Om man sänker temperaturen hos luft sjunker mättnadstrycket för
vattenĺnga sĺ att det kan hamna under det ĺngtryck som finns i luften.
Vid 293 K är vattenĺngans mättnadstryck 2.4 kPa och tätheten för
mättad ĺnga är 17.5 g/m3.Men om luften bara innehĺller 40 % av den
vattenmängden d v s om ĺngans täthet bara är 0.4*17.5 = 7 g/m3 blir
även ĺngans tryck 40 % av mättnadstrycket d v s 1 kPa.Vi säger dĺ
att relativa fuktigheten är 40 %.Med realtiv fuktighet menas alltsĺ
vattenĺngans patialtryck i procent av vattenĺngans mättnadstryck.
Om vi har luft med 40 % relativ fuktighet vid temperaturen 293 K är
alltsĺ ĺngans tryck 1 kPa och varje m3 fuktig luft innehĺller 7 g
vatten.Sänker vi temperaturen sjunker mättnadstrycket vilket innebär
att den relativa fuktigheten stiger.Vid c:a 280 K blir mättnadstrycket
1 kPa vilket innebär att den relativa fuktigheten blir 100 %.
Detta sätt att räkna är inte helt korrekt eftersom tätheten för mättad
ĺnga inte är helt proportionell mot trycket.Ĺngtätheten vid 280 K är
7.8 och man kan faktiskt sänka temperaturen till 279 K innan man nĺr
100 % relativ fuktighet.Men för praktiska uppskattningar är metoden
oftast användbar.
Fortsätter vi att sänka temperaturen kommer vatten att kondensera.Det
kan ske vid en vattenyta men det är ocksĺ möjligt att vatten kondenserar
till smĺ droppar som svävar i luften.Luft med sĺdana smĺ droppar kallas
dimma eller moln.Den temperatur där vatten börjar falla ut i vätskeform
kallas för daggpunkten.
När vatten förĺngas (eller kondenserar) omsätts värme.Detta värme kallas
ĺngbildningsvärme och kan delas upp i tre delar:
1 När vatten övergĺr till ĺnga ökar volymen.Denna volymökning sker
vid mättnadstryck och innebär ett arbete PV där P=mättnadstryck
och V=volymökning.Detta arbete mĺste motsvaras av lika stor
energitillförsel i form av värme om temperaturen skall förbli
konstant.
2 När vattenmolekylerna lämnar vätskan kan de röra sig friare.Antalet
frihetsgrader d v s entropin ökar.För att hĺlla konstant temperatur
mĺste vi tillföra energi till dessa nya frihetsgrader.Vi mĺste
tillföra energin TS där T=temperaturen och S=entropiökningen.
3 Bindningarna mellan molekylerna i vätskan (eller isen) mĺste brytas
för att molekyler skall kunna lämna vätskan.Detta kräver värmetill-
försel.
1 kg vatten som förĺngas vid 293 K ger 58 m3 ĺnga vid 2.3 kPa (volymen
pĺ utgĺngsvätskan är försumbar).Volymökning pĺ 58 m3 vid 2.3 kPa ger ett
arbete pĺ 133 kJ.Men för att förĺnga detta vatten mĺste vi tillföra
ĺngbildningsvärmet d v s 2451 kJ.Det ĺtgĺr alltsĺ 2451 - 133 = 2318 kJ
för att öka antalet frihetsgrader och för att bryta molekylbindningar.
För att förĺnga 1 kg vatten vid 293 K mĺste man alltsĺ tillföra 2451 kJ värme
vid den konstanta temperaturen 293 K.Entropin hos detta tillförda värme blir
alltsĺ 2451/293 = 8.37 kJ/K.
Vatten är nödvändigt för allt liv och tillgĺng till vatten är alltsĺ en
förutsättning för att en plats skall vara beboelig.Och praktiskt taget
över allt pĺ jorden finns vatten tillgängligt i form av vattenĺnga i
luften.Även torr ökenluft innehĺller vatten.Med sĺ lĺg relativ fuktighet
som 10 % innehĺller het ökenluft vid 323 K (50 oC) 8 g vatten per m3.
En luftkonditioneringsanläggning för ett hus pĺ 200 m3 som ĺstadkommer
en halv luftomsättnig per timme hanterar 100 m3 per timme d v s
800 g vatten per timme.En sĺdan anläggning skulle alltsĺ kunna konden-
sera ut ett par hinkar vatten per dygn.Tillräckligt för ett hushĺlls behov
av dricksvatten.
För att underlätta uppskattningar av vattenupptag och vattenutfällning för
luft har jag kompletterat programmet för Allmänna gaslagen med uppskattningar
för fuktig luft (t v fungerar endast isokor och isoterm).
Använd programmet för fuktberäkningar med försiktighet!
Dels är det mycket troligt att det finns direkta felskrivningar i källkoden,
dels har jag använt en hel del ungefärliga uppskattningar,dels är förloppen
inte entydigt beskrivna av starttillstĺnd och sluttillstĺnd,dels kan
kondensation och förĺngning ta tid sĺ att jämvikt inte hinner inställa sig
i praktiken,dels fungerar programmet bara i temperaturintrvallet 273 - 373 K.
För att ladda ner programmet för Allmänna gaslagen klickar du pĺ nedanstĺende
rubrik
___________________________________
-----------------------
Ĺter till Tekniksida
 Fig 1
Fig 1
 Fig 2
Om du,när du drar ut kolven till läge d öppnar ett hĺl i kolven
sĺ att luft kan komma in kommer du att fĺ atmosfärstryck inne
i sprutan.Det medför att ĺngbildningen inte blir lika häftig.Om
temperaturen är under 373 K kommer vattenet inte att koka.Men
att vattenytan bombarderas med luftmolekyler pĺverkar inte
balansen mellan frisättning och bindning av vattenmolekyler.
Sĺ smĺningom kommer vi till att ĺngtrycket blir mättnadstrycket,
totala trycket blir atmosfärstryck och den torra luftens tryck
blir atmosfärstryck minus mättnadstryck.
Om du stänger hĺlet i kolven och skjuter in den komprimeras
luften praktiskt taget enligt allmänna gaslagen och ĺngtrycket
blir mättnadstrycket.Totala trycket i sprutan blir det resulterande
lufttrycket plus ĺngtrycket.
Fig 2
Om du,när du drar ut kolven till läge d öppnar ett hĺl i kolven
sĺ att luft kan komma in kommer du att fĺ atmosfärstryck inne
i sprutan.Det medför att ĺngbildningen inte blir lika häftig.Om
temperaturen är under 373 K kommer vattenet inte att koka.Men
att vattenytan bombarderas med luftmolekyler pĺverkar inte
balansen mellan frisättning och bindning av vattenmolekyler.
Sĺ smĺningom kommer vi till att ĺngtrycket blir mättnadstrycket,
totala trycket blir atmosfärstryck och den torra luftens tryck
blir atmosfärstryck minus mättnadstryck.
Om du stänger hĺlet i kolven och skjuter in den komprimeras
luften praktiskt taget enligt allmänna gaslagen och ĺngtrycket
blir mättnadstrycket.Totala trycket i sprutan blir det resulterande
lufttrycket plus ĺngtrycket.
 Fig 3
Den torra luften fyller ut den tillgängliga volymen.Vattenĺngan fyller
ut den tillgängliga volymen.Den torra luftens tryck och vattenĺngans
tryck adderas och summan blir den fuktiga luftens tryck.
Den torra luftens tryck kallas partialtrycket för den torra luften
och ĺngans tryck kallas ĺngans partialtryck.Det totala trycket är
summan av alla partialtryck.
Ĺngtrycket över en vattenyta är alltsĺ lika med mättnadstrycket,om
temperaturen har varit konstant sĺ länge att det rĺder balans mellan
förĺngning och kondensation vid vattenytan.Men för den luft som
omger oss avviker ĺngtrycket ofta frĺn mättnadstryck av tvĺ orsaker.
1 Det finns inget vatten i närheten som kan förĺngas
2 Temperaturen har nyligen ändrats
Om man sänker temperaturen hos luft sjunker mättnadstrycket för
vattenĺnga sĺ att det kan hamna under det ĺngtryck som finns i luften.
Vid 293 K är vattenĺngans mättnadstryck 2.4 kPa och tätheten för
mättad ĺnga är 17.5 g/m3.Men om luften bara innehĺller 40 % av den
vattenmängden d v s om ĺngans täthet bara är 0.4*17.5 = 7 g/m3 blir
även ĺngans tryck 40 % av mättnadstrycket d v s 1 kPa.Vi säger dĺ
att relativa fuktigheten är 40 %.Med realtiv fuktighet menas alltsĺ
vattenĺngans patialtryck i procent av vattenĺngans mättnadstryck.
Om vi har luft med 40 % relativ fuktighet vid temperaturen 293 K är
alltsĺ ĺngans tryck 1 kPa och varje m3 fuktig luft innehĺller 7 g
vatten.Sänker vi temperaturen sjunker mättnadstrycket vilket innebär
att den relativa fuktigheten stiger.Vid c:a 280 K blir mättnadstrycket
1 kPa vilket innebär att den relativa fuktigheten blir 100 %.
Detta sätt att räkna är inte helt korrekt eftersom tätheten för mättad
ĺnga inte är helt proportionell mot trycket.Ĺngtätheten vid 280 K är
7.8 och man kan faktiskt sänka temperaturen till 279 K innan man nĺr
100 % relativ fuktighet.Men för praktiska uppskattningar är metoden
oftast användbar.
Fortsätter vi att sänka temperaturen kommer vatten att kondensera.Det
kan ske vid en vattenyta men det är ocksĺ möjligt att vatten kondenserar
till smĺ droppar som svävar i luften.Luft med sĺdana smĺ droppar kallas
dimma eller moln.Den temperatur där vatten börjar falla ut i vätskeform
kallas för daggpunkten.
När vatten förĺngas (eller kondenserar) omsätts värme.Detta värme kallas
ĺngbildningsvärme och kan delas upp i tre delar:
1 När vatten övergĺr till ĺnga ökar volymen.Denna volymökning sker
vid mättnadstryck och innebär ett arbete PV där P=mättnadstryck
och V=volymökning.Detta arbete mĺste motsvaras av lika stor
energitillförsel i form av värme om temperaturen skall förbli
konstant.
2 När vattenmolekylerna lämnar vätskan kan de röra sig friare.Antalet
frihetsgrader d v s entropin ökar.För att hĺlla konstant temperatur
mĺste vi tillföra energi till dessa nya frihetsgrader.Vi mĺste
tillföra energin TS där T=temperaturen och S=entropiökningen.
3 Bindningarna mellan molekylerna i vätskan (eller isen) mĺste brytas
för att molekyler skall kunna lämna vätskan.Detta kräver värmetill-
försel.
1 kg vatten som förĺngas vid 293 K ger 58 m3 ĺnga vid 2.3 kPa (volymen
pĺ utgĺngsvätskan är försumbar).Volymökning pĺ 58 m3 vid 2.3 kPa ger ett
arbete pĺ 133 kJ.Men för att förĺnga detta vatten mĺste vi tillföra
ĺngbildningsvärmet d v s 2451 kJ.Det ĺtgĺr alltsĺ 2451 - 133 = 2318 kJ
för att öka antalet frihetsgrader och för att bryta molekylbindningar.
För att förĺnga 1 kg vatten vid 293 K mĺste man alltsĺ tillföra 2451 kJ värme
vid den konstanta temperaturen 293 K.Entropin hos detta tillförda värme blir
alltsĺ 2451/293 = 8.37 kJ/K.
Vatten är nödvändigt för allt liv och tillgĺng till vatten är alltsĺ en
förutsättning för att en plats skall vara beboelig.Och praktiskt taget
över allt pĺ jorden finns vatten tillgängligt i form av vattenĺnga i
luften.Även torr ökenluft innehĺller vatten.Med sĺ lĺg relativ fuktighet
som 10 % innehĺller het ökenluft vid 323 K (50 oC) 8 g vatten per m3.
En luftkonditioneringsanläggning för ett hus pĺ 200 m3 som ĺstadkommer
en halv luftomsättnig per timme hanterar 100 m3 per timme d v s
800 g vatten per timme.En sĺdan anläggning skulle alltsĺ kunna konden-
sera ut ett par hinkar vatten per dygn.Tillräckligt för ett hushĺlls behov
av dricksvatten.
För att underlätta uppskattningar av vattenupptag och vattenutfällning för
luft har jag kompletterat programmet för Allmänna gaslagen med uppskattningar
för fuktig luft (t v fungerar endast isokor och isoterm).
Fig 3
Den torra luften fyller ut den tillgängliga volymen.Vattenĺngan fyller
ut den tillgängliga volymen.Den torra luftens tryck och vattenĺngans
tryck adderas och summan blir den fuktiga luftens tryck.
Den torra luftens tryck kallas partialtrycket för den torra luften
och ĺngans tryck kallas ĺngans partialtryck.Det totala trycket är
summan av alla partialtryck.
Ĺngtrycket över en vattenyta är alltsĺ lika med mättnadstrycket,om
temperaturen har varit konstant sĺ länge att det rĺder balans mellan
förĺngning och kondensation vid vattenytan.Men för den luft som
omger oss avviker ĺngtrycket ofta frĺn mättnadstryck av tvĺ orsaker.
1 Det finns inget vatten i närheten som kan förĺngas
2 Temperaturen har nyligen ändrats
Om man sänker temperaturen hos luft sjunker mättnadstrycket för
vattenĺnga sĺ att det kan hamna under det ĺngtryck som finns i luften.
Vid 293 K är vattenĺngans mättnadstryck 2.4 kPa och tätheten för
mättad ĺnga är 17.5 g/m3.Men om luften bara innehĺller 40 % av den
vattenmängden d v s om ĺngans täthet bara är 0.4*17.5 = 7 g/m3 blir
även ĺngans tryck 40 % av mättnadstrycket d v s 1 kPa.Vi säger dĺ
att relativa fuktigheten är 40 %.Med realtiv fuktighet menas alltsĺ
vattenĺngans patialtryck i procent av vattenĺngans mättnadstryck.
Om vi har luft med 40 % relativ fuktighet vid temperaturen 293 K är
alltsĺ ĺngans tryck 1 kPa och varje m3 fuktig luft innehĺller 7 g
vatten.Sänker vi temperaturen sjunker mättnadstrycket vilket innebär
att den relativa fuktigheten stiger.Vid c:a 280 K blir mättnadstrycket
1 kPa vilket innebär att den relativa fuktigheten blir 100 %.
Detta sätt att räkna är inte helt korrekt eftersom tätheten för mättad
ĺnga inte är helt proportionell mot trycket.Ĺngtätheten vid 280 K är
7.8 och man kan faktiskt sänka temperaturen till 279 K innan man nĺr
100 % relativ fuktighet.Men för praktiska uppskattningar är metoden
oftast användbar.
Fortsätter vi att sänka temperaturen kommer vatten att kondensera.Det
kan ske vid en vattenyta men det är ocksĺ möjligt att vatten kondenserar
till smĺ droppar som svävar i luften.Luft med sĺdana smĺ droppar kallas
dimma eller moln.Den temperatur där vatten börjar falla ut i vätskeform
kallas för daggpunkten.
När vatten förĺngas (eller kondenserar) omsätts värme.Detta värme kallas
ĺngbildningsvärme och kan delas upp i tre delar:
1 När vatten övergĺr till ĺnga ökar volymen.Denna volymökning sker
vid mättnadstryck och innebär ett arbete PV där P=mättnadstryck
och V=volymökning.Detta arbete mĺste motsvaras av lika stor
energitillförsel i form av värme om temperaturen skall förbli
konstant.
2 När vattenmolekylerna lämnar vätskan kan de röra sig friare.Antalet
frihetsgrader d v s entropin ökar.För att hĺlla konstant temperatur
mĺste vi tillföra energi till dessa nya frihetsgrader.Vi mĺste
tillföra energin TS där T=temperaturen och S=entropiökningen.
3 Bindningarna mellan molekylerna i vätskan (eller isen) mĺste brytas
för att molekyler skall kunna lämna vätskan.Detta kräver värmetill-
försel.
1 kg vatten som förĺngas vid 293 K ger 58 m3 ĺnga vid 2.3 kPa (volymen
pĺ utgĺngsvätskan är försumbar).Volymökning pĺ 58 m3 vid 2.3 kPa ger ett
arbete pĺ 133 kJ.Men för att förĺnga detta vatten mĺste vi tillföra
ĺngbildningsvärmet d v s 2451 kJ.Det ĺtgĺr alltsĺ 2451 - 133 = 2318 kJ
för att öka antalet frihetsgrader och för att bryta molekylbindningar.
För att förĺnga 1 kg vatten vid 293 K mĺste man alltsĺ tillföra 2451 kJ värme
vid den konstanta temperaturen 293 K.Entropin hos detta tillförda värme blir
alltsĺ 2451/293 = 8.37 kJ/K.
Vatten är nödvändigt för allt liv och tillgĺng till vatten är alltsĺ en
förutsättning för att en plats skall vara beboelig.Och praktiskt taget
över allt pĺ jorden finns vatten tillgängligt i form av vattenĺnga i
luften.Även torr ökenluft innehĺller vatten.Med sĺ lĺg relativ fuktighet
som 10 % innehĺller het ökenluft vid 323 K (50 oC) 8 g vatten per m3.
En luftkonditioneringsanläggning för ett hus pĺ 200 m3 som ĺstadkommer
en halv luftomsättnig per timme hanterar 100 m3 per timme d v s
800 g vatten per timme.En sĺdan anläggning skulle alltsĺ kunna konden-
sera ut ett par hinkar vatten per dygn.Tillräckligt för ett hushĺlls behov
av dricksvatten.
För att underlätta uppskattningar av vattenupptag och vattenutfällning för
luft har jag kompletterat programmet för Allmänna gaslagen med uppskattningar
för fuktig luft (t v fungerar endast isokor och isoterm).